La Comisión Europea ha autorizado el uso de Leqembi, el innovador fármaco desarrollado por las farmacéuticas Eisai y Biogen, para el tratamiento de pacientes con Alzheimer en sus primeras etapas. Esta decisión convierte al medicamento en el primero aprobado por la Unión Europea que ataca directamente la causa subyacente de esta devastadora enfermedad neurodegenerativa, marcando un punto de inflexión en la lucha contra el deterioro cognitivo.
Leqembi: el primer tratamiento aprobado en la UE que aborda la raíz del Alzheimer
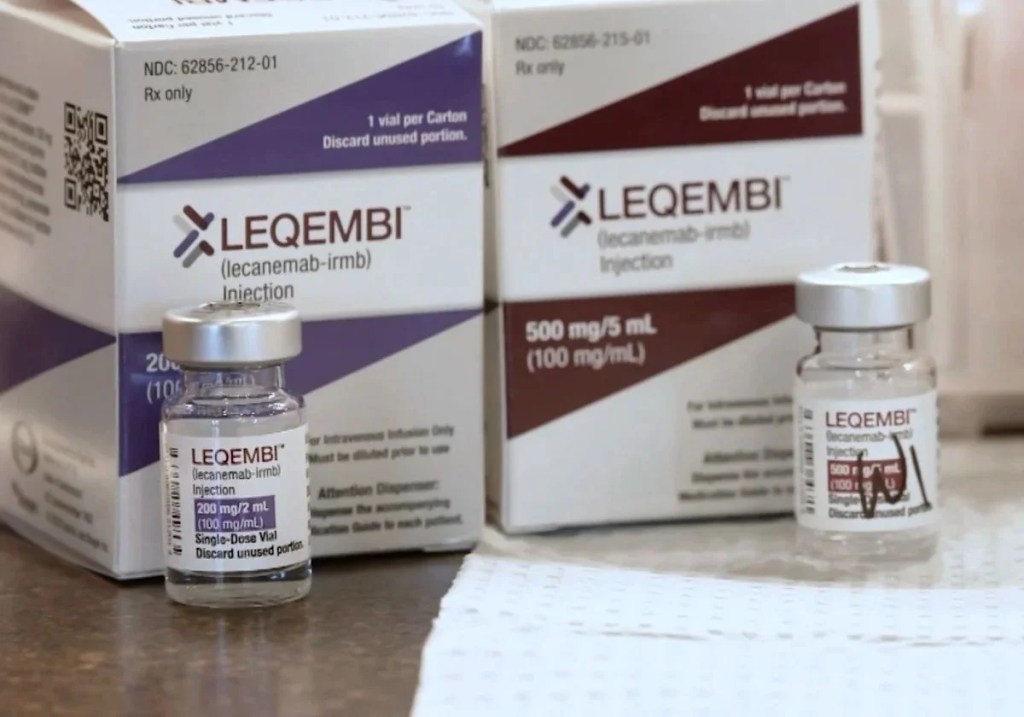
Tras un proceso de evaluación que se extendió por más de dos años, la Comisión Europea ha dado luz verde a Leqembi, un fármaco cuyo objetivo no es solo mitigar los síntomas del Alzheimer, sino frenar su progresión desde las fases iniciales. Esto representa un cambio radical en el paradigma de tratamiento de una enfermedad que afecta a millones de personas en Europa.
Leqembi actúa sobre la proteína beta amiloide, una sustancia que forma placas pegajosas en el cerebro y que es considerada una de las principales causas del Alzheimer. La acumulación de esta proteína interfiere con la comunicación neuronal, llevando al deterioro progresivo de la memoria, la orientación y otras funciones cognitivas. Al eliminar o reducir esta sustancia, el fármaco busca preservar la salud cerebral durante más tiempo y mejorar la calidad de vida de los pacientes en etapas tempranas.
Sin embargo, la aprobación no es generalizada: el medicamento solo será autorizado para personas que tengan una o ninguna copia del gen ApoE4, y que presenten depósitos de beta amiloide en el cerebro. Esta restricción responde a preocupaciones de seguridad, ya que estudios previos indicaron que los pacientes con dos copias del gen tendrían un mayor riesgo de efectos secundarios graves, como inflamación cerebral.
Un fármaco prometedor, pero con cautela regulatoria

La decisión europea se alinea con la recomendación reciente de la Agencia Europea de Medicamentos (EMA), que ya había respaldado el uso limitado de Leqembi a un subconjunto específico de pacientes. Inicialmente, la EMA mostró resistencia a su aprobación debido a los posibles riesgos asociados, lo que provocó una nueva ronda de evaluación de seguridad por parte de la Comisión Europea antes de tomar una decisión definitiva.
Priya Singhal, jefa de desarrollo de Biogen, declaró que tanto su compañía como Eisai están “actuando con urgencia” para poner Leqembi a disposición de los pacientes europeos lo antes posible. Esta celeridad refleja no solo la demanda médica, sino también el impacto emocional y económico que representa el Alzheimer tanto para los pacientes como para sus familias.
En contraste, el fármaco rival de Eli Lilly fue rechazado recientemente por la EMA debido a que sus beneficios no compensaban los riesgos de seguridad identificados, lo que refuerza la importancia del equilibrio entre eficacia clínica y seguridad en el tratamiento de enfermedades neurológicas complejas.
Mientras tanto, Leqembi ya ha sido aprobado en otros importantes mercados como Estados Unidos, Japón, China, Reino Unido y varios países adicionales. En Estados Unidos, incluso está aprobado para pacientes con dos copias del gen ApoE4, aunque se exige la realización de escáneres cerebrales periódicos para detectar posibles efectos adversos tempranos.
Analistas del sector, como Myles Minter de William Blair, estiman que las ventas de Leqembi podrían superar los 900 millones de dólares hacia la década de 2030, reflejando la alta expectativa del mercado ante un medicamento que representa un verdadero avance terapéutico.
Con la aprobación de Leqembi, Europa da un paso crucial en la lucha contra el Alzheimer, ofreciendo una nueva esperanza a los pacientes en etapas tempranas de la enfermedad. Aunque su uso será restringido a ciertos perfiles genéticos por motivos de seguridad, este hito representa un avance significativo hacia tratamientos más efectivos y personalizados para uno de los mayores desafíos de salud pública del siglo XXI.
Referencia:
- Comisión Europea/Commission authorises medicine for treatment of early Alzheimer’s disease. Link.
Relacionado
Descubre más desde Cerebro Digital
Suscríbete y recibe las últimas entradas en tu correo electrónico.

0 Comments